基于阵列电极的破损环氧涂层失效演变行为研究
时间:
摘要:涂层保护是金属腐蚀防护的关键方法之一。但是对于破损涂层来说,由于涂层/金属界面的封闭性,腐蚀性介质在涂层/金属界面扩散引起的涂层失效一直是各国学者争相研究的热点。因此采用阵列电极测试方法,结合电化学测试方法,建立了腐蚀性介质在涂层/金属界面上扩散引起的涂层失效过程。结果表明:涂层失效过程分为两个阶段:随着腐蚀性介质在涂层/金属界面上的扩散,体系的阳极区不断增大,涂层覆盖区域和未覆盖区域的电位差和电流密度差均减小,此时电化学阻抗特征表现为扩散阻抗,形成了界面为阳极、涂层未覆盖区为阴极的氧浓差电池;随着实验的进行,在氧浓差腐蚀的作用下,涂层完全失效,体系电位分布和电流密度分布与涂层无关。
关键词:阵列电极;破损涂层;电化学阻抗;失效
金属腐蚀问题不仅仅会带来大量金属损失,也会引起诸多的安全隐患[1-3]。金属防护一直是各国学者争相研究的热点。而有机涂层防护技术广泛应用于金属防护领域,从最初的石油沥青防腐层到如今的氟碳漆等多种涂层,而有机环氧涂层以其较高的交联密度、高强度等优点广泛应用于金属防护领域[4-7]。但是在现场实际环境中,当有机涂层发生破损,腐蚀性介质从破损处进入到涂层/金属界面并且发生扩散时,极易引起涂层和金属的失效。但由于涂层/金属界面的封闭性,涂层/金属体系的失效过程难以描述,也就导致了无法采取相关的措施对涂层/金属界面进行防护。而阵列电极技术在描述体系整体电位、电流密度分布特征等方面具有巨大的优势[8]。因此本文以DGEBA环氧涂层构建破损涂层体系为研究对象,通过阵列电极技术、电化学测试技术研究了涂层失效的全过程,以期为涂层/金属界面防护研究提供借鉴。
1实验设置
1.1阵列电极
阵列电极制备:以透明有机玻璃板为基础,采用精雕机加工10×10的阵列圆孔,孔径为2mm,小孔之间的间距为0.5mm;当打磨至光亮的直径为2mm的X80钢丝插入到小孔内并与有机玻璃板平行。采用环氧树脂对阵列电极进行封装,保证钢丝之间完全绝缘。室温固化72h后打磨阵列电极,使之完全漏出X80钢金属基体,最后通过金相砂纸打磨电极至平整,以减小由于表面粗糙度不同引起的实验误差;将处理后的阵列电极放入真空干燥箱中备用。
相关知识推荐:化工方面的核心期刊都有哪些
涂层制备:实验涂层采用高分子DGEBA环氧涂层(双酚A缩水甘油醚),手工喷涂至阵列电极表面(50%),室温固化168h后,采用五点测试法[9]确定其涂层厚度为(10±2)μm。
电位和电流密度数据采集:编写Labview程序,通过数据采集卡实现不同实验时间条件下的阵列电极电位和电流密度值的自动采集,实验周期为72h。
1.2电化学测试
涂层体系制备:以X80钢试片(25×25×2mm2)为基体,依次采用丙酮除油、去离子水清洗和酒精除水后,干燥放入真空干燥箱中备用;使用前,在背面焊接一根测试导线,通过环氧树脂封装,只留下一个面积为25×25mm2的工作面;实验前,采用金相砂纸打磨至镜面,手工涂覆环氧涂层,室温固化168h后采用五点测试法确定其涂层厚度为(10±2)μm;通过数字精雕机在试样表面制造一个直径为2mm的圆孔,露出金属基体,形成破损涂层环境。
电化学测试:采用电化学工作站开展电化学阻抗测试,测试频率范围为105~10-2Hz,扰动电压为±10mV,数据处理采用ZSimpWin软件。
实验条件:采用分析纯NaCl和去离子水配制质量分数为3%的NaCl实验溶液,整个实验装置放置于恒温恒湿箱中,实验温度设置为25℃。
2结果与讨论
2.1涂层表面电位和电流密度分布研究
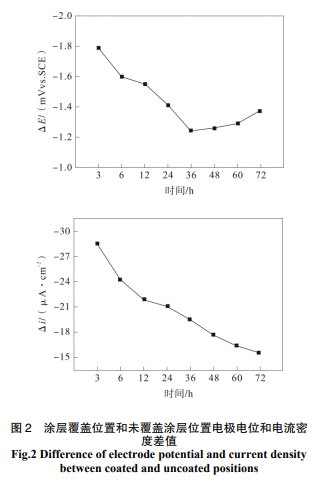
图1为破损环氧涂层表面电位和电流密度分布随时间的变化规律;图2为层覆盖位置和未覆盖涂层位置电极电位和电流密度差值。
随着腐蚀性介质对破损涂层体系的侵蚀,可以看出,在实验时间为3h时,未覆盖区域的金属电位整体上明显负于涂层覆盖区域金属电位,同时由于腐蚀性介质在涂层/金属界面上的扩散,涂层覆盖区域涂层电位逐渐发生负向偏移,由初始时刻的阴极区向阳极区转变。随着时间的推移,当实验时间进行到12h时,未覆盖区域金属电位持续负向偏移,同时由于腐蚀性介质在界面上的扩散,整个体系的阳极区增大;在后续的12h里,从电位表面分布图像可以看出,电位分布分为涂层覆盖和未覆盖两个明显的区域,从表面电位分布图像可以看出,电位整体差异性减小,由于界面上缝隙的封闭结构,整个区域形成了氧浓差电池,腐蚀加剧。
从图2可以看出,此时腐蚀性介质在界面上扩散、形成氧浓差电池的时间为36h,此时覆盖区域和未覆盖区域的整体电位差持续降低,而随后两个区域内的电位差值略有增大但基本保持不变,从72h的电位表面分布曲线可以看出,此时覆盖涂层体系完全失效,涂层表面电位分布差异与涂层无关,而与金属表面的状态有关。从电流密度的表面分布来说,在0~36h内,整个电流分布以覆盖区域和未覆盖区域分为明显的两个区域,而当实验进行到72h时,整个表面区域性不明显,涂层完全失效;而从图2电流差异曲线可以看出,随着实验的进行,电流差异逐渐减小,说明整个区域内由于腐蚀性介质在涂层/金属界面的扩散,涂层逐渐失效,即涂层覆盖区域金属逐渐暴露在腐蚀性界面中,最终涂层完全失效。
2.2界面电化学扩散过程研究
图3为破损涂层体系的电化学阻抗响应特征曲线。在整个实验周期内,不考虑水的扩散对界面上的影响,因此根据拟合电路和测试结果发现,整个反应过程(0~72h)主要包含两个阶段。
第一阶段为0~24h。从图3中可以看出,随着实验的进行,在1h时,阻抗图表现为1/4容抗弧与扩散阻抗相连[10],因此选择等效电路Rs(Qc(RcW(CdlRct))):Rs为溶液电阻,Qc为体系电容,Rc为体系电阻,W为韦伯扩散阻抗,Cdl为双电层电容,Rct为电荷转移电阻。这表明此时电解质已经逐步在界面上发生扩散:中性溶液中阴极主要发生吸氧反应O2+2H2O+4e-→4OH-,阳极Fe→Fe2++2e-;当实验进行到12h时,整个过程依然是以扩散为主,没有形成明显的扩散通道/缝隙,此时表现为涂层电容Cc增大,电阻降低,扩散阻抗表现为“不理想”(n≈0.75)的韦伯阻抗。当实验进行到24h时,依然存在扩散阻抗尾巴,但是容抗弧直径明显减小,此时涂层电容与扩散阻抗均明显增大,说明此时氧浓差电池正在逐渐形成,而电解质中的氧气也逐渐消耗殆尽,金属表面双电层逐渐形成。
第二阶段为36~72h。当实验进行到36h时,此时图中扩散阻抗已经消失,基本表现为1/4容抗特征,此时进入到第二阶段,因此选择等效电路Rs(Qc(Rc(CdlRct)))。随着反应的进行,氧浓差电池已经形成,此时缝内只发生金属的溶解和水解Fe+2H2O→Fe(OH)2+2H++2e-;在后续的时间内,整个体系以氧浓差腐蚀机理为主。
图4为不同频率下阻抗和相位角变化曲线。根据相位角和阻抗的测试数据可以发现,整个实验过程可以分为两个阶段。在第一阶段(0~24h),当频率f=0.5Hz时出现最大相位角,也就是“峰”值,此时低频区域表现为“不理想的”的电容特征,根据上述分析可知,此时n≈0.75,溶液向涂层/金属界面上的扩散已经发生,并且在存在人为制造破损孔的条件下,其“完美”的涂层电容性质已经被打破,这也是导致在测试初期整个测试频率范围内相位角偏离90°的主要原因[11]。等效电路拟合结果见表1。
当实验进行到第二阶段时,在36h测试点处,最大相位角相比于24h时有微小增加。从图3可以发现,在36h时,体系的电容值发生明显增大,此时腐蚀缝隙和双电层逐步形成[12]。随着实验时间的增加,均在频率f=0.07Hz时出现最大相位角,且逐渐减小,这也意味着在这一阶段主要以缝隙内的氧浓差腐蚀过程为主。
3结论
本文通过阵列电极结合电化学阻抗测试方法,分析了腐蚀性介质在金属/涂层界面扩散引起的破损涂层失效问题,主要得到以下结论:
1)随着腐蚀性介质对破损涂层体系的侵蚀,在0~36h内,覆盖区域和未覆盖区域分为明显的阴极区和阳极区,但是两者的电位差逐渐减小;在36~72h内,由于氧浓差电池的形成,涂层失效,涂层覆盖区域金属完全暴露于腐蚀性介质中,此时表面电位和电流分布与涂层无关。
2)随着腐蚀性介质扩散,在第一阶段(0~36h)电化学阻抗表现为扩散特征,表现为腐蚀性介质在界面上的扩散过程及氧浓差电池形成过程;当进入到第二阶段(36~72h),涂层失效,电化学阻抗特征为双容抗弧的金属腐蚀特征。——论文作者:钱宇1,温航2

 >
>