局部进展期胃癌行腹腔热灌注化疗的疗效与安全性分析
时间:
目的 探讨腹腔热灌注化疗(HIPEC)在局部进展期胃癌(LAGC)患者中的疗效和安全性。
方法 采用单中心回顾性分析,纳入2019年1月至2023年12月接受根治性切除术的206例LAGC患者。根据患者是否接受HIPEC分为HIPEC组(n=105)和非HIPEC组(n=101)。所有患者接受R0切除并进行术后辅助化疗。HIPEC组患者于术后第3天和第5天行HIPEC治疗。主要观察指标包括总生存期(OS)、无复发生存期(RFS)和不良反应。
结果 Kaplan-Meier生存曲线分析显示,两组OS比较,差异无统计学意义(P=0.099,HR=0.670, 95%CI: 0.415~1.081),但HIPEC组患者2年和3年OS生存率分别为92.4%和86.7%,显著高于非HIPEC组的76.2%和74.3%(P=0.001和P=0.024)。在RFS方面,HIPEC组患者的RFS优于非HIPEC组(P=0.049, HR=0.690, 95%CI: 0.476~1.001),HIPEC组2年和3年的RFS分别为78.1%和70.5%,显著高于非HIPEC组的63.4%和54.5%(P=0.020和P=0.018)。两组术后并发症发生率及肿瘤标志物(CEA、CA19-9、AFP)水平在术后各时间点比较,差异均无统计学意义(P>0.05)。
结论 HIPEC可显著改善LAGC患者的RFS,并在长期OS方面展现出潜在获益。尽管在总体OS上未达统计学显著性,但HIPEC仍显示出良好的疗效与安全性。未来研究应进一步优化HIPEC治疗策略,并探索其联合其他疗法的可能性,以改善患者长期预后。
关键词: 腹腔热灌注化疗;局部进展期胃癌;总生存期;无复发生存期;不良反应
论文《局部进展期胃癌行腹腔热灌注化疗的疗效与安全性分析》发表在《肿瘤药学》,版权归《肿瘤药学》所有。本文来自网络平台,仅供参考。
0 前言
胃癌是全球范围内发病率和死亡率均居前列的消化系统恶性肿瘤之一,在我国尤为高发[1]。局部进展期胃癌(locally advanced gastric cancer, LAGC)患者虽可通过根治性切除术实现病灶清除,但术后仍存在较高的腹膜复发风险[2]。研究表明,腹腔内游离癌细胞及微小残留病灶是导致术后复发和远处转移的关键因素,其检出率可达20%~40%[3-4]。因此,如何在围手术期有效清除腹腔内潜在癌细胞、降低复发风险,已成为当前胃癌综合治疗研究的关键问题。
腹腔热灌注化疗(hyperthermic intraperitoneal chemotherapy, HIPEC)是一种在腹腔内循环灌注化疗药物并将液体温度控制在41~43℃的治疗方法[5-7]。热疗与化疗的协同作用可增强细胞膜通透性、抑制DNA修复并提高药物敏感性,从而在腹腔内形成高药物浓度、低系统毒性的局部治疗环境,有效杀灭残余癌细胞。近年来,HIPEC已被应用于伴有腹膜转移的胃癌及高危患者的术中辅助治疗,并显示出一定的防复发潜力。
然而,目前HIPEC在LAGC治疗中的临床获益与安全性仍缺乏高质量循证医学证据,各研究中心在适应证选择、药物方案及操作流程方面亦存在较大差异。本研究聚焦LAGC患者术后复发风险控制和治疗方案优化,通过回顾性分析接受根治性手术的LAGC患者,比较HIPEC联合手术及辅助化疗与常规手术联合辅助化疗在治疗效果和安全性方面的差异,旨在为HIPEC在LAGC治疗中的临床应用提供科学依据,推动胃癌治疗方案的优化,并可能有助于改善患者的长期生存预后,从而为胃癌术后治疗策略的临床实施提供实践支持。
1 资料与方法
1.1 研究对象
本研究为单中心回顾性分析,纳入2019年1月至2023年12月接受根治性切除术的LAGC患者共206例,根据术中是否接受HIPEC分为HIPEC组(n=105)和非HIPEC组(n=101)。
1.2 纳入与排除标准
纳入标准:(1)经病理学确诊为胃腺癌;(2)术后病理分期为T3~T4期、任何N分期且无远处转移(M0);(3)接受R0根治性切除术;(4)术前未接受放化疗。
排除标准:(1)存在肝、肺、骨或脑等远处转移;(2)术前曾接受放化疗或靶向治疗;(3)合并其他恶性肿瘤;(4)临床资料或随访信息不完整。
1.3 手术及HIPEC方案
所有患者均行根治性胃切除术,包括全胃或远端胃切除,并行D2淋巴结清扫。HIPEC组患者于术后第3天和第5天各进行一次HIPEC。采用闭式循环系统,灌注药物为紫杉醇75 mg·m⁻²,灌注液以2 L·m⁻²加温生理盐水配制,经热交换器加热至43°C后于腹腔内循环灌注60 min,流速控制在400~500 mL·min⁻¹。两次灌注间隔48 h,监测患者体温、心率及引流液变化。非HIPEC组患者仅行根治性切除术,不进行HIPEC。
1.4 术后辅助化疗
两组患者均于术后4~6周接受静脉化疗,方案为奥沙利铂联合S-1(SOX方案),每3周为1个周期,共治疗6~8个周期,根据患者耐受情况调整化疗剂量。
1.5 观察指标
收集患者术前一般资料,术前及术后检测血清肿瘤标志物水平,并记录不良反应发生情况。主要观察指标包括:术后并发症发生率;复发方式与复发时间;总生存期(overall survival, OS)与无复发生存期(recurrence-free survival, RFS)。随访通过门诊及电话进行,截至2025年10月。
1.6 统计学分析
使用SPSS 26.0和R 4.2.1软件进行统计学分析。计量资料以“均数±标准差”(x±s)表示,组间比较采用t检验或Mann-Whitney U检验。计数资料以百分率(%)表示,组间比较采用χ²检验或Fisher确切概率法。生存分析采用Kaplan-Meier法绘制生存曲线,组间差异比较采用Log-rank检验。在亚组分析中,采用Cox回归模型评估T分期、N分期和病理分化程度等变量对OS和RFS的独立影响。以P<0.05为差异有统计学意义。
2 结果
2.1 一般临床资料
两组患者年龄、性别、体重指数、肿瘤部位、分化程度、T分期和N分期等基线特征比较,差异均无统计学意义(P>0.05),具有可比性(表1)。
表1 两组患者临床病理特征比较
(表格内容略,详见原文)
2.2 不良反应
两组患者胃肠道反应(食欲缺乏、恶心呕吐、腹泻)、骨髓抑制(白细胞减少、血小板减少)、电解质紊乱(低钠血症、低钾血症)、肝功能异常和肾功能异常等不良反应发生率比较,差异均无统计学意义(P>0.05)(表2)。
表2 两组患者不良反应比较[例(%)]
(表格内容略,详见原文)
2.3 术后并发症
HIPEC组和非HIPEC组吻合口瘘、腹腔感染、肠梗阻的发生率及并发症总发生率比较,差异均无统计学意义(P>0.05)(表3)。
表3 两组患者术后并发症比较[例(%)]
(表格内容略,详见原文)
2.4 肿瘤标志物
两组患者术前血清CEA、CA19-9和AFP水平比较,差异均无统计学意义(P>0.05);术后3、6、9个月时,两组上述各指标均较术前呈下降趋势,但下降幅度相似,差异均无统计学意义(P>0.05),提示HIPEC治疗未引起术后肿瘤标志物水平的显著波动(表4)。
表4 两组患者术前及术后肿瘤标志物水平比较
(表格内容略,详见原文)
2.5 总生存期(OS)
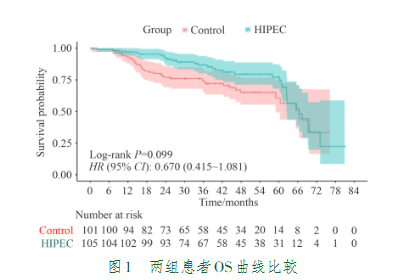
Kaplan-Meier生存曲线显示,两组患者的OS比较,差异无统计学意义(P=0.099, HR=0.670, 95%CI: 0.415~1.081)(图1)。进一步分析表明,HIPEC组1年OS率为96.2%,非HIPEC组为93.1%,差异无统计学意义(P=0.319);HIPEC组2年OS率为92.4%,显著高于非HIPEC组的76.2%(P=0.001);HIPEC组3年OS率为86.7%,显著高于非HIPEC组的74.3%(P=0.024),表明HIPEC治疗可显著提高患者的长期OS率(表5)。
图1 两组OS曲线比较
表5 两组患者OS比较[例(%)]
(图表内容略,详见原文)
2.6 无复发生存期(RFS)
Kaplan-Meier生存曲线显示,HIPEC组患者的RFS优于非HIPEC组(P=0.049, HR=0.690, 95% CI: 0.476~1.001)(图2)。进一步分析表明,HIPEC组1年RFS率为88.6%,非HIPEC组为83.2%,差异无统计学意义(P=0.265);HIPEC组2年RFS率为78.1%,显著高于非HIPEC组的63.4%(P=0.020)。HIPEC组3年RFS率为70.5%,显著高于非HIPEC组的54.5%(P=0.018),表明HIPEC治疗可显著改善患者的RFS率(表6)。
图2 两组RFS曲线比较
表6 两组患者RFS比较[例(%)]
(图表内容略,详见原文)
2.7 OS和RFS亚组分析
亚组分析显示,在T4期、N2~N3期及未分化/低分化胃癌患者中,HIPEC治疗显著改善了OS与RFS(P<0.05);而在T3期、N0~N1期及中/高分化胃癌患者中,HIPEC未显示出明显的生存获益(P>0.05)(表7)。
表7 LAGC患者OS和RFS的亚组分析
(表格内容略,详见原文)
3 讨论
本研究通过回顾性分析探讨了HIPEC在LAGC患者中的疗效与安全性。结果表明,HIPEC治疗能够显著改善患者的RFS,尽管两组间OS的差异无统计学意义,但HIPEC组RFS显著优于对照组。这些结果为HIPEC在LAGC患者术后辅助治疗中的应用提供了临床依据,并为其在降低肿瘤复发率、改善患者预后方面的潜在价值提供了新的证据支持。
本研究聚焦于HIPEC在LAGC中的预防性应用,即在尚无明确远处转移的患者中探讨其疗效,而目前多数研究集中于已出现腹膜转移的胃癌患者。以治疗性HIPEC为例,Langellotti等[8]的系统综述指出,胃癌腹膜转移患者接受肿瘤细胞减灭术联合HIPEC后,OS为9.8~28.2个月,显著优于传统姑息化疗组,提示HIPEC对存在腹膜转移的患者具有生存获益。本研究发现,在尚未发生远处转移的LAGC患者中应用HIPEC,RFS的改善更为显著,提示早期干预可能具有更优的临床获益。此外,有研究指出,患者选择因素(如腹膜癌指数低、可达完全细胞减灭、病灶数目少)对HIPEC的疗效具有重要影响[9]。因此,本研究结果与上述观点一致,均提示在经筛选的患者群体中HIPEC具有治疗优势,但其能否最终转化为OS的显著改善,仍需延长随访时间或扩大样本量进一步验证。
研究表明,HIPEC的应用未显著增加术后常见并发症(如吻合口瘘、腹腔感染和肠梗阻等)的发生率[10]。本研究中,两组术后并发症发生率无显著差异,表明HIPEC在安全性方面表现良好。虽然HIPEC可能会引起胃肠道不适和轻微的骨髓抑制反应,但上述不良反应大多可逆,未对患者造成长期不良影响。
亚组分析结果显示,HIPEC在T4、N2~N3等高肿瘤负荷分期及低分化/未分化患者中呈现出更明显的生存获益;而在T3、N0~N1期及中/高分化等相对低风险分层中,HIPEC的治疗效应并不显著。值得注意的是,未达到统计学显著疗效并不等同于“无效”,更可能与亚组分层后样本量减少、结局事件发生数下降、统计效能不足及回顾性研究固有的残余混杂因素有关。总体而言,上述结果提示,未来研究可采用风险富集策略,优先在T4、N2~N3期等腹膜复发高风险人群中进一步验证HIPEC的潜在增益。鉴于本研究的亚组分析属于小样本探索性分析,其结论仍需在独立队列及前瞻性研究中进一步验证。
本研究结果显示,HIPEC的潜在获益更可能集中于复发风险较高的LAGC人群,尤其是T4、N2~N3期及低分化/未分化患者。上述特征提示更高的腹膜播散与腹腔微小残留病灶风险,因此更适合作为未来进行“风险富集”与分层验证研究的核心依据。相较之下,在相对低风险亚组中未观察到明确的获益信号,提示HIPEC的临床价值可能并非适用于所有LAGC患者,需通过更精准的人群选择来优化获益-风险比。HIPEC的获益信号更可能出现在T4、N2~N3期等高风险分层,未来研究应采用前瞻性随机对照设计,在统一系统治疗背景下评估HIPEC的增量价值,终点设置宜优先反映腹膜相关复发控制(如RFS或腹膜复发结局),并同步纳入OS、安全性、系统治疗完成率及生活质量等综合指标。与此同时,对治疗路径的标准化与中心间质量控制将是保障结论可解释性与可推广性的关键。
本研究证实,HIPEC对LAGC的复发具有显著抑制作用,其作用机制主要涉及热疗与化疗药物的协同效应、对肿瘤微环境的重塑、药物渗透性增强及机体抗肿瘤免疫反应的激活等多个层面。首先,热疗可显著提高肿瘤细胞膜通透性,增强药物渗透和细胞内积聚,从而提升化疗药物的杀伤效能,并通过诱导细胞凋亡有效清除腹腔中的微小残留病灶[11-12]。其次,HIPEC在腹腔内形成的高温化疗环境不仅具有直接的细胞毒作用,还能通过抑制DNA修复、干扰蛋白折叠及线粒体功能,进一步增强肿瘤细胞对药物的敏感性。同时,腹腔灌注过程本身的机械冲洗效应可减少腹膜表面的肿瘤细胞附着和再种植,从而有效预防腹膜转移的发生[14]。此外,HIPEC的热应激还可改变肿瘤微环境,促进肿瘤抗原释放,并增强抗肿瘤免疫反应。上述机制共同构成了HIPEC的生物学基础,使其在控制局部残余病灶、抑制腹膜种植及改善长期预后方面具有显著优势,为其在LAGC围手术期辅助治疗中的推广提供了坚实的理论依据。
尽管本研究结果显示HIPEC可显著改善LAGC患者的RFS,但在OS方面的长期改善尚未达到统计学显著性,提示未来研究应进一步探讨HIPEC的优化策略,特别是在治疗时机、频次、药物选择等方面,同时可考虑将HIPEC与其他新型治疗方法(如靶向治疗、免疫治疗等)联合应用,以期进一步提高患者的生存获益。此外,随着肿瘤分子生物学的发展,个体化治疗将成为未来研究的重点。患者的基因型、肿瘤的分子特征等因素可能会影响HIPEC的疗效,因此制定个体化治疗方案对于提高HIPEC的治疗效果至关重要。生物标志物,尤其是肿瘤标志物和分子标志物,在评估患者对HIPEC的反应和制定个体化治疗方案中具有重要意义。肿瘤标志物(如CEA、CA19-9、AFP等)及分子标志物(如癌基因突变、抑癌基因、微小RNA等)不仅可为疗效预测提供依据,还有助于识别对HIPEC反应较好的患者,从而优化治疗方案。未来的研究可进一步探索新的生物标志物,以便早期评估治疗效果并为患者术后监测提供支持。
本研究的局限性包括:本研究为单中心回顾性设计,可能存在选择偏倚;HIPEC组和非HIPEC组在某些基线特征上的差异可能影响结果的普遍性。此外,部分患者随访时间较短,且在治疗策略、样本量等方面尚存在改进空间。因此,未来仍需开展多中心、大样本量的前瞻性随机对照试验对本研究结果进行验证。
本研究表明,HIPEC可显著改善LAGC患者的RFS,并在OS方面展现出一定的积极作用,同时具有良好的安全性。未来研究应进一步优化HIPEC治疗策略,并结合其他治疗方法,以期进一步提高LAGC患者的长期生存率。
参考文献
[1] BRAY F, LAVERSANNE M, SUNG H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2024, 74(3): 229-263. DOI: 10.3322/caac.21834.
[2] JIAO X G, WANG Y, WANG F, et al. Recurrence pattern and its predictors for advanced gastric cancer after total gastrectomy[J]. Medicine, 2020, 99(51): e23795. DOI: 10.1097/MD.0000000000023795.
[3] JAMEL S, MARKAR SR, MALIETZIS G, et al. Prognostic significance of peritoneal lavage cytology in staging gastric cancer: systematic review and meta-analysis[J]. Gastric Cancer, 2018, 21(1): 10-18. DOI: 10.1007/s10120-017-0749-y.
[4] CIESLA S, LISIECKI R, &AWNICKA A, et al. Clinical significance of peritoneal fluid examination for free cancer cells in patients scheduled for surgery for gastric cancer[J]. Front Surg, 2021, 8: 685868. DOI: 10.3389/fsurg.2021.685868.
[5] RAMIREZ M F, GUERRA-LONDONO J J, OWUSU-AGYEMANG P, et al. Temperature management during cytoreductive surgery with hyperthermic intraperitoneal chemotherapy[J]. Front Oncol, 2023, 12: 1062158. DOI: 10.3389/fonc.2022.1062158.
[6] TONELLO M, CENZI C, PIZZOLATO E, et al. National guidelines for cytoreductive surgery and hyperthermic intraperitoneal chemotherapy (HIPEC) in peritoneal malignancies: a worldwide systematic review and recommendations of strength analysis[J]. Ann Surg Oncol, 2025, 32(8): 5795-5806. DOI: 10.1245/s10434-025-17518-z.
[7] PELC Z, SEDLAK K, ENDO Y, et al. Hyperthermic intraperitoneal chemotherapy (HIPEC) for gastric cancer with peritoneal metastasis-Joint analysis of European GASTRODATA and American national cancer database[J]. Am J Surg, 2025, 242: 116235. DOI: 10.1016/j.amjsurg.2025.116235.
[8] LANGELLOTTI L, FIORILLO C, D'ANNIBALE G, et al. Efficacy of cytoreductive surgery (CRS) + HIPEC in gastric cancer with peritoneal metastasis: systematic review and meta-analysis[J]. Cancers, 2024, 16(10): 1929. DOI: 10.3390/cancers16101929.
[9] CHIA C S, SESHADRI R A, KEPENEKIAN V, et al. Survival outcomes after cytoreductive surgery and hyperthermic intraperitoneal chemotherapy for peritoneal carcinomatosis from gastric cancer: a systematic review[J]. Pleura Peritoneum, 2016, 1(2): 67-77. DOI: 10.1515/pp-2016-0010.
[10] LIU L, ZHENG L B, LIU S L, et al. Prognostic analysis of prophylactic hyperthermic intraperitoneal chemotherapy for advanced gastric cancer: a propensity score-matched analysis[J]. J Gastrointest Surg, 2023, 27(12): 2790-2801. DOI: 10.1007/s11605-023-05823-5.
[11] BEEHARRY M K, LIU W T, YAO X X, et al. A critical analysis of the cytoreductive surgery with hyperthermic intraperitoneal chemotherapy combo in the clinical management of advanced gastric cancer: an effective multimodality approach with scope for improvement[J]. Transl Gastroenterol Hepatol, 2016, 1: 77. DOI: 10.21037/tgh.2016.08.05.
[12] DELLINGER T H, HAN E S, RAOOF M, et al. Hyperthermic intraperitoneal chemotherapy-induced molecular changes in humans validate preclinical data in ovarian cancer[J]. JCO Precis Oncol, 2022, 6: e2100239. DOI: 10.1200/PO.21.00239.
[13] CHIA D K A, DEMUYTERE J, ERNST S, et al. Effects of hyperthermia and hyperthermic intraperitoneal chemoperfusion on the peritoneal and tumor immune contexture[J]. Cancers, 2023, 15(17): 4314. DOI: 10.3390/cancers15174314.
[14] ACS M, PISO P, GLOCKZIN G. Peritoneal metastatic gastric cancer: local treatment options and recommendations[J]. Curr Oncol, 2024, 31(3): 1445-1459. DOI: 10.3390/curroncol31030109.
[15] GWEE Y X, CHIA D K A, SO J, et al. Integration of genomic biology into therapeutic strategies of gastric cancer peritoneal metastasis[J]. J Clin Oncol, 2022, 40(24): 2830. DOI: 10.1200/JCO.21.02745.

 >
>